Вероятно, не одна сотня тысяч лет прошла с тех пор, как люди познакомились с огнем и научились сами получать теплоту. Каждый из нас грелся у горячей печки и мерз в стужу. Казалось бы, что может быть привычнее и понятнее, чем знакомая всем теплота. Но сказать, что такое теплота, не просто. Правильный ответ на этот вопрос наука нашла не так уж давно.
Две гипотезы о природе теплоты. Природу теплоты объяснили бесспорным и очевидным как будто бы фактом: при нагревании системы ее температура повышается,- значит, система получает «что-то». При остывании, охлаждаясь, система отдает «что-то». Это «что-то» было названо теплотой.
О природе теплоты были высказаны две гипотезы. Первой гипотезы придерживался Галилей (1613). Теплота - это вещество. Оно необычно, способно проникать в любые тела и выходить из них. Тепловое вещество, иначе теплород, не порождается и не уничтожается, а только перераспределяется между телами. При увеличении количества теплорода в теле температура повышается, при уменьшении - понижается. При полном отсутствии теплорода в теле достигается наименьшая возможная температура - абсолютный нуль температуры.
Первоначально сторонники гипотезы теплорода считали (потом Блек заставил их переменить взгляды), что термометр измеряет количество теплорода в теле. Само слово «температура» в переводе с латинского означает смесь. Когда-то, например, о бронзе говорили, что она «температура олова и меди». Под температурой тела понимали смесь из материи тела и теплорода. Градус температуры (до второй половины 18 в. говорили, согласно существовавшим представлениям, градус теплоты) выражал крепость этой смеси. (До сих пор сохранился обычай мерить в градусах крепость вина - смесь воды и спирта.)

Рис. 9. Под сильными ударами молота нагревается и начинает светиться железная полоса. Под ударами выжимается теплород из полосы, как вода из губки, утверждает одна гипотеза. Удары приводят в движение мельчайшие частицы железа, утверждает другая гипотеза.
Второй гипотезы придерживался (1620) английский философ Ф. Бэкон (1561 - 1626). Он обратил внимание на то, что знал любой кузнец: под сильными ударами молота холодный кусок железа становится горячим. Известен был также способ получения огня трением. Бэкон из этого заключил: теплота есть внутреннее движение мельчайших частиц тела и температура тела определяется скоростью движения частиц в нем. Эта теория называется механической теорией теплоты. Эту теорию во многом обосновал и развил (1748) гениальный М. В. Ломоносов (1711 - 1765).
М. В. Ломоносов обосновывает существование абсолютного нуля температуры с позиции второй гипотезы. Нулю соответствует уже не полное отсутствие теплорода в теле, но полное прекращение движения частиц. Развитие науки подтвердит существование абсолютного нуля, хотя и отвергнет представление о полном прекращении движения частиц при абсолютном нуле.
При всем коренном различии обе гипотезы сходятся в очень важном. Вещество ли теплота или движение, в обоих случаях количество теплорода в системе или количество движения в ней вполне определяется состоянием системы. Обе гипотезы приводят к одинаковому выводу: теплота независимо от ее природы - свойство системы. Обе гипотезы позволяют говорить о количестве теплоты, содержащейся в системе. По обеим гипотезам, изменение количества теплоты в системе определяется только начальным и конечным состояниями системы и не зависит от пути перехода системы из начального состояния в конечное.
О работе уже писали: работа не содержится в системе; работа не есть свойство системы; количество работы в общем случае зависит от пути перехода системы из начального состояния в конечное. В 19 в. наука придет к очень важному выводу: теплота тоже не содержится в системе; теплота тоже не есть свойство системы. Поэтому обе гипотезы окажутся неверными. Первая гипотеза отпадает полностью. Вторая же гипотеза, как выяснится, применима не к теплоте, а к совсем другой величине. Эту величину впоследствии назвали тепловой (термической) энергией системы.
Экспериментальная проверка гипотезы теплорода. Выдающийся современный биолог Т. Добжанский указал: «Хорошая гипотеза побуждает ставить опыты. Они же или подтверждают гипотезу, или же показывают ее ошибочность. История науки свидетельствует о том, что некоторые гипотезы, отброшенные впоследствии как ошибочные, тем не менее оказались полезными: они побудили к хорошим экспериментальным исследованиям». Хочется думать; что биолог имел в виду гипотезу теплорода. Лучший пример трудно отыскать. Раньше всего проверили допущение, что термометр измеряет крепость смеси из материи и теплорода. Опыты провели в 1661 г. француз Морен, в 1720 г. - крупный английский математик Б. Тейлор (1685 - 1731) и в 1750 г.- выдающийся русский физик Г. В. Рихман (1711 - 1753).
Читатели не пети удодовы и решат задачу: смешивают разные количества двух сортов вина различной крепости. Каков градус вина после смешения? В частности, при смешении одинаковых количеств вина разной крепости градус смеси равен полусумме исходных градусов. Тейлор и Рихман смешивали не вино, а различные количества воды разной температуры и измеряли температуру воды после смешения. Их расчетная формула (формула Тейлора - Рихмана) была такой же, как при решении задач на градусы вина. В частности, при смешении одинаковых количеств воды, имеющих разные температуры, конечная температура смеси равнялась полусумме начальных температур.
Опыты не только с водой, но и с другими жидкостями подтвердили правильность формулы Тейлора - Рихмана. Как будто бы хорошо? Но по словам знаменитого французского писателя Франсуа Вольтера (1694 - 1778), «теории подобны мышам, они проходят через девять дыр и застревают в десятой». Формула Тейлора - Рихмана «застряла» на опытах по определению температуры, которая устанавливается при встряхивании воды и ртути. Эти опыты провел (1732) Фаренгейт по предложению очень известного в свое время голландского врача и химика Бургаве (1668 - 1738). Температура при встряхивании равных масс воды и ртути не равна среднему арифметическому начальных температур воды и ртути.
Теплоемкость. Результат опыта Фаренгейта - Бургаве противоречит формуле Тейлора - Рихмана. Но теорию не отбрасывают полностью при первом же противоречащем ей опыте. Теорию изменяют, стараясь спасти в ней главное. Блек (1760) объяснил опыт Фаренгейта - Бургаве. Блек придерживался гипотезы теплорода, но отверг представление, что термометр измеряет крепость смеси из материи и теплорода. При встряхивании воды и ртути количество теплоты, полученной одной жидкостью, равно количеству теплоты, отданной другой. Это - главное в теории теплорода. По измерениям Фаренгейта, равные количества теплоты различно изменяют температуру у равных масс воды и ртути. Значит, у равных масс воды и ртути различные емкости для теплоты. Этот термин предложил Блек. Сейчас говорят «теплоемкость». Теплоемкость измеряют количеством теплоты, сообщаемой телу для увеличения его температуры на один градус (по выбранной шкале температур). При массе тела в одну единицу теплоемкость называется удельной, при произвольной массе тела - общей. Общая теплоемкость равна удельной, умноженной на массу тела.
Опыты Фаренгейта - Бургаве позволяют вычислить отношение удельных теплоемкостей двух несмешивающихся жидкостей. Но в 1780 г. предложили приравнять удельную теплоемкость воды единице. Приравнивание удельной теплоемкости воды единице устанавливает и единицу теплоты. При повышении температуры одного грамма воды на один градус по шкале Цельсия, с 14.5'С до 15,5'С (теплоемкость зависит от температуры), вода получает одну единицу теплоты, одну малую калорию (кал). Само название «калория» появилось в 1852 г. Одна тысяча малых калорий составляет одну большую калорию (Ккал).
Введение понятия теплоемкости явилось одним из крупнейших успехов в истории термодинамики.
Скрытая теплота. Представление о том, что термометр измеряет крепость смеси из материи и теплорода, привело к двум выводам. Первый вывод: удельные теплоемкости всех тел при равных температурах одинаковы. Этот вывод опроверг Блек. Второй вывод: крепость не может измениться без изменения температуры. Тело не может ни получить, ни отдать теплоту при постоянной температуре. Блек опроверг и этот вывод. Он обнаружил скрытые (термин Блека) теплоты плавления (1761) и испарения (1764).
Блек измерил скрытую теплоту плавления льда по методу смешения. Он налил в стеклянный сосуд известной массы известное количество воды и нагрел сосуд и воду до одной и той же температуры. Она была выше температуры плавления льда. Далее Блек ввел в воду определенную массу льда при температуре его плавления и после расплавления льда и установления термического равновесия измерил конечную температуру. Она была ниже первоначальной температуры стеклянного сосуда и воды в нем, но выше температуры плавления льда. Проведенный затем расчет предполагал (не начинать расчета, не уяснив предположения!), что количество теплоты при смешении не изменилось, а только перераспределилось. Стеклянный сосуд и вода в нем отдали теплоту; лед и образовавшаяся из него вода получили теплоту (такое же количество). Удельная теплоемкость стекла (отнесенная к удельной теплоемкости воды как единице) была известна. Поэтому по температуре стеклянного сосуда и воды до опыта и конечной их температуре рассчитывают количества теплоты, потерянные сосудом и водой. Для расплавления льда надо было сообщать ему скрытую теплоту плавления (без изменения температуры), а затем теплоту для нагрева образовавшейся воды от температуры плавления льда до конечной температуры. Задача логически решена, и остаются несложные вычисления.
Открытие Блеком скрытой теплоты испарения идейно тесно связано с открытием скрытой теплоты плавления.
Блек похоронил представление, что термометр измеряет крепость смеси из материи и теплорода. Недаром сказано: Гораздо легче измерять, чем точно знать, что измеряется». Блек отделил понятие температуры от понятия теплоты. Температуру теперь рассматривают как свойство системы, от которого зависят условия термического равновесия, внутреннего и внешнего. Температура определяет условия наступления термического равновесия. При непосредственном контакте двух систем с различными температурами более высокая температура понижается, а более низкая температура повышается. При таком контакте теплота переходит от системы с более высокой температурой к системе с более низкой температурой. Так характеризовал температуру выдающийся английский физик Дж. К. Максвелл (1831 - 1879).
Термохимия. Открытия Блека - триумф теории теплорода. Они сохранят все свое первостепенное значение и после падения этой теории, но будут иначе истолкованы.
Блек был практикующим врачом. Задолго до Блека и долго после него для развития термодинамики много делали врачи. Специальность врача располагала к самостоятельным наблюдениям и выводам. Новый триумф теории теплорода опять был обязан врачу, русскому академику Г. И. Гессу (1802 - 1850).
Блек, а вслед за ним и другие исследователи использовали скрытую теплоту для целей калориметрии, т. е. для измерения количества теплоты. Количество теплоты, отданной льду, прямо пропорционально массе растаявшего льда. Исходный лед и образовавшаяся вода должны находиться при температуре плавления льда.
А. Л. Лавуазье (1743 - 1794) и П. С. Лаплас (1749 - 1827) усовершенствовали ледяной калориметр и измерили (1782 - 1784) количества теплоты, которые выделяются при окислении пищи кислородом и при дыхании морской свинки. В обоих случаях образуется двуокись углерода. Количества теплоты, отнесенные к единице массы двуокиси углерода, были одного и того же порядка. Даже примерное совпадение значений доказывало, что выделение теплоты животным вызвано окислением пищи в организме животного кислородом. «Жизнь - химическое действие», - заключил Лавуазье.
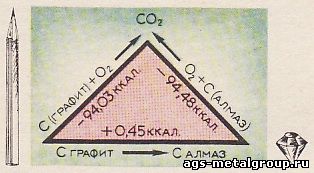
Рис. 10. Тепловой эффект превращения графита в алмаз. На опыте его измерить нельзя, но легко подсчитать по закону Гесса. Нужно знать, какое количество теплоты выделяется при окислении одного моля углерода как в виде графита, так и в виде алмаза. Разность между их теплотами горения и равна теплоте превращения графита в алмаз.
В 1840 г. Гесс открыл закон постоянства тепловых сумм - вершина калориметрических исследований в 19 в. «Если образуется соединение, то количество выделившейся теплоты является постоянным, независимо от того, образуется ли соединение непосредственно или через промежуточные соединения», - писал Гесс. Вывод закона Гесса явно опирается на положение, что количество теплоты не изменяется.
Трудно переоценить значение закона Гесса для химической термодинамики. Прямое измерение количества теплоты (теплового эффекта) при протекании огромного большинства химических реакций составило бы крайне сложную, едва ли выполнимую экспериментальную задачу. Закон Гесса позволяет заменить прямое измерение несравненно более простыми измерениями на обходных путях (рис. 10).
Успехи теории теплорода были велики. Но объяснений всем известным явлениям эта теория или не давала, или давала с большой натяжкой. Рассказ об этих явлениях в следующей главе.
